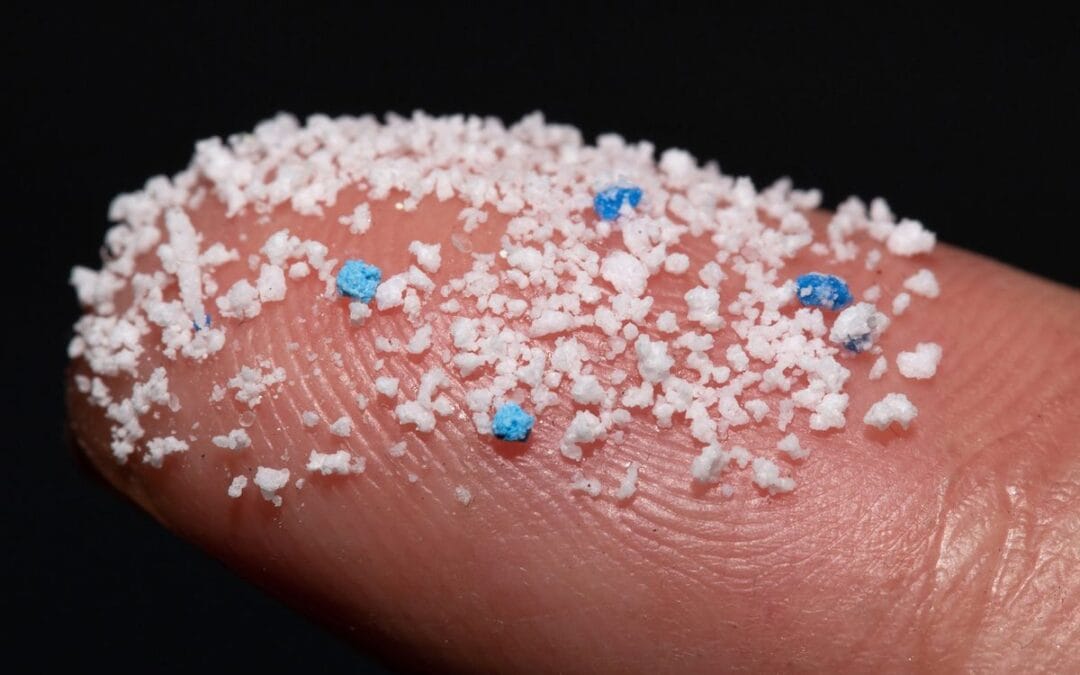
La medicina moderna ha avanzado de forma significativa en el control de infecciones, el diseño de biomateriales y la optimización de técnicas quirúrgicas. Sin embargo, paralelamente, han surgido nuevos factores ambientales que comienzan a ser relevantes para la práctica clínica. Uno de ellos es la creciente presencia de microplásticos en el organismo, un fenómeno que ya no se limita al ámbito ambiental y que empieza a mostrar implicaciones biológicas directas, particularmente en procesos críticos como la regeneración de heridas y la regeneración tisular.
Evidencia experimental reciente sugiere que los microplásticos no son partículas inertes, sino agentes capaces de interferir con rutas celulares esenciales para la cicatrización, lo que podría traducirse en tiempos de recuperación más prolongados y mayor riesgo de complicaciones postquirúrgicas (Shen et al., 2025).
Evidencia científica emergente
Un estudio publicado en NanoImpact analizó el efecto de microplásticos de poliestireno en modelos murinos con heridas cutáneas, tanto en condiciones fisiológicas normales como en un modelo de diabetes experimental, un escenario clínicamente relevante por su conocida dificultad para la cicatrización (Shen et al., 2025).
Los resultados fueron consistentes: los animales expuestos a microplásticos presentaron un retraso significativo en el cierre de heridas, acompañado de una alteración profunda en los mecanismos celulares responsables de la regeneración del tejido. Este efecto fue aún más marcado en el contexto diabético, donde la capacidad de reparación ya está comprometida.
Entre los hallazgos clave, se observó una disminución en la proliferación y migración de fibroblastos, células fundamentales para la formación de matriz extracelular y el cierre efectivo de la herida. Asimismo, se documentó una reducción en la angiogénesis, proceso indispensable para el aporte de oxígeno y nutrientes al tejido en reparación, y una menor deposición de colágeno, lo que compromete la resistencia y calidad del tejido regenerado (Shen et al., 2025).
Mecanismos moleculares implicados
El valor de este estudio radica en que no se limita a una observación fenotípica, sino que profundiza en los mecanismos moleculares que explican este deterioro en la cicatrización. Los autores identificaron que la exposición a microplásticos altera la expresión de la enzima NAT10, provocando una desregulación epigenética que impacta directamente sobre la vía FASN–PI3K/AKT (Shen et al., 2025).
La vía PI3K/AKT es ampliamente reconocida por su papel en la supervivencia celular, el metabolismo energético y la regeneración tisular. Su inhibición se traduce en una menor capacidad de las células para proliferar, migrar y responder al estrés tisular. En términos prácticos, esto significa que el microambiente de la herida se vuelve menos favorable para una reparación eficiente.
Adicionalmente, la alteración de FASN afecta la síntesis de lípidos, un proceso crítico para la formación de membranas celulares y la expansión de células involucradas en la regeneración. Este desequilibrio metabólico refuerza la hipótesis de que los microplásticos pueden reprogramar negativamente la respuesta biológica del tejido lesionado (Shen et al., 2025).

Imagen: Cero Residuo
Relevancia clínica y riesgos potenciales
Aunque estos hallazgos provienen de modelos animales, su relevancia clínica es directa. La cicatrización de heridas es un proceso altamente conservado entre especies, y los mecanismos celulares afectados en este estudio son los mismos que participan en la recuperación postquirúrgica.
En pacientes con diabetes, infecciones óseas, cirugías ortopédicas complejas o trauma, cualquier factor que prolongue la inflamación o interfiera con la fase proliferativa puede traducirse en mayores tiempos de hospitalización, incremento del riesgo infeccioso y peores resultados funcionales. La posible contribución de contaminantes ambientales como los microplásticos introduce una variable adicional que merece atención en el análisis integral del paciente.
Este enfoque resulta particularmente relevante en un contexto donde ya se ha demostrado la presencia de microplásticos en sangre y tejidos humanos. Aunque aún faltan estudios clínicos que correlacionen directamente niveles de exposición con resultados en cicatrización, la evidencia preclínica establece un marco biológico plausible que no puede ser ignorado (Shen et al., 2025).
Implicaciones para la innovación terapéutica y el control del riesgo infeccioso
A la luz de esta evidencia, la gestión del microambiente tisular adquiere un papel central en la recuperación clínica, particularmente en escenarios donde factores externos —como la exposición a microplásticos— pueden interferir con los mecanismos normales de reparación. En este contexto, estrategias terapéuticas orientadas al control local de la carga bacteriana y a la estabilización del entorno de la herida se vuelven críticas para mitigar riesgos adicionales que prolonguen la inflamación o retrasen la regeneración.
Soluciones como Stimulan, diseñadas para actuar como transportador local de antibiótico, permiten abordar de forma directa uno de los principales factores que comprometen la cicatrización: la infección persistente o subclínica. Al facilitar una liberación controlada y localizada del antibiótico en el sitio de la lesión, este tipo de tecnología contribuye a reducir la presión infecciosa sin depender exclusivamente de concentraciones sistémicas, favoreciendo un entorno más estable para la reparación tisular.
En escenarios complejos —como cirugía ortopédica, trauma o infecciones óseas— donde la regeneración ya enfrenta múltiples desafíos, el control eficaz del microambiente local puede funcionar como un factor compensatorio frente a interferencias externas que alteran la respuesta biológica del tejido. Más que un soporte mecánico, este enfoque prioriza la protección activa del proceso de cicatrización, permitiendo que las rutas celulares involucradas en la regeneración operen en condiciones más favorables y predecibles.
Conclusión
El estudio de Shen et al. (2025) aporta evidencia sólida de que los microplásticos pueden interferir activamente en la cicatrización de heridas, afectando rutas celulares y metabólicas críticas para la regeneración tisular. Para la práctica clínica y el desarrollo de soluciones médicas, estos hallazgos subrayan una realidad emergente: la recuperación del paciente está influida no solo por la técnica o el producto utilizado, sino por un entorno biológico cada vez más complejo.
En este contexto, apostar por estrategias terapéuticas y dispositivos médicos que favorezcan una recuperación eficiente, controlada y resistente a factores externos deja de ser una ventaja competitiva y se convierte en una necesidad clínica.
Referencias
Shen, F. J., Liu, Y., Zhang, Y., Wang, Z., Li, X., & Chen, Y. (2025). Microplastics impair wound healing via NAT10-mediated epigenetic dysregulation of FASN-PI3K/AKT signaling. NanoImpact, 37, 100497. https://pubmed.ncbi.nlm.nih.gov/40889597/